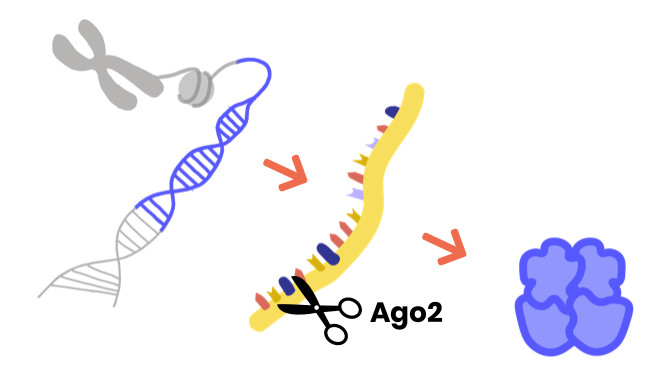
Die Veränderung des AGO1/2-Gens erfolgte auf natürliche Weise und wurde nicht durch Lebensstil, Ernährung oder andere Umweltfaktoren verursacht. Die Veränderung trat zufällig entweder im Sperma oder in der Eizelle eines Elternteils oder während der frühen Entwicklung des Embryos nach der Vereinigung von Ei- und Samenzelle auf. Wenn Sie Eltern eines betroffenen Menschen sind, sollten Sie wissen, dass Sie nichts falsch gemacht haben!
Wir alle haben zwei Kopien von jedem Argonauten-Gen. Eine Mutation in nur einer der beiden Kopien von AGO1/2 kann die Störung verursachen ("autosomal dominant").
Bei den meisten Menschen, bei denen die Krankheit bisher diagnostiziert wurde, haben beide Elternteile die gleiche genetische Veränderung in AGO1/2. Genetische Veränderungen, die bei beiden Elternteilen nicht vorkommen, werden als "de novo"-Mutationen bezeichnet.
Wenn die Veränderung "de novo" auftrat, ist die Wahrscheinlichkeit, dass sie bei einem anderen Kind wieder auftritt, sehr gering. In seltenen Fällen tragen mehrere Ei- oder Samenzellen dieselbe genetische Veränderung (gonadaler Mosaizismus), und dann kann sie an ein Kind weitergegeben werden. Wenn Sie möchten, können Sie während der Schwangerschaft mittels Fruchtwasseruntersuchung auf eine AGO1/AGO2-Genveränderung testen. Fragen Sie einen klinischen Genetiker um Rat.